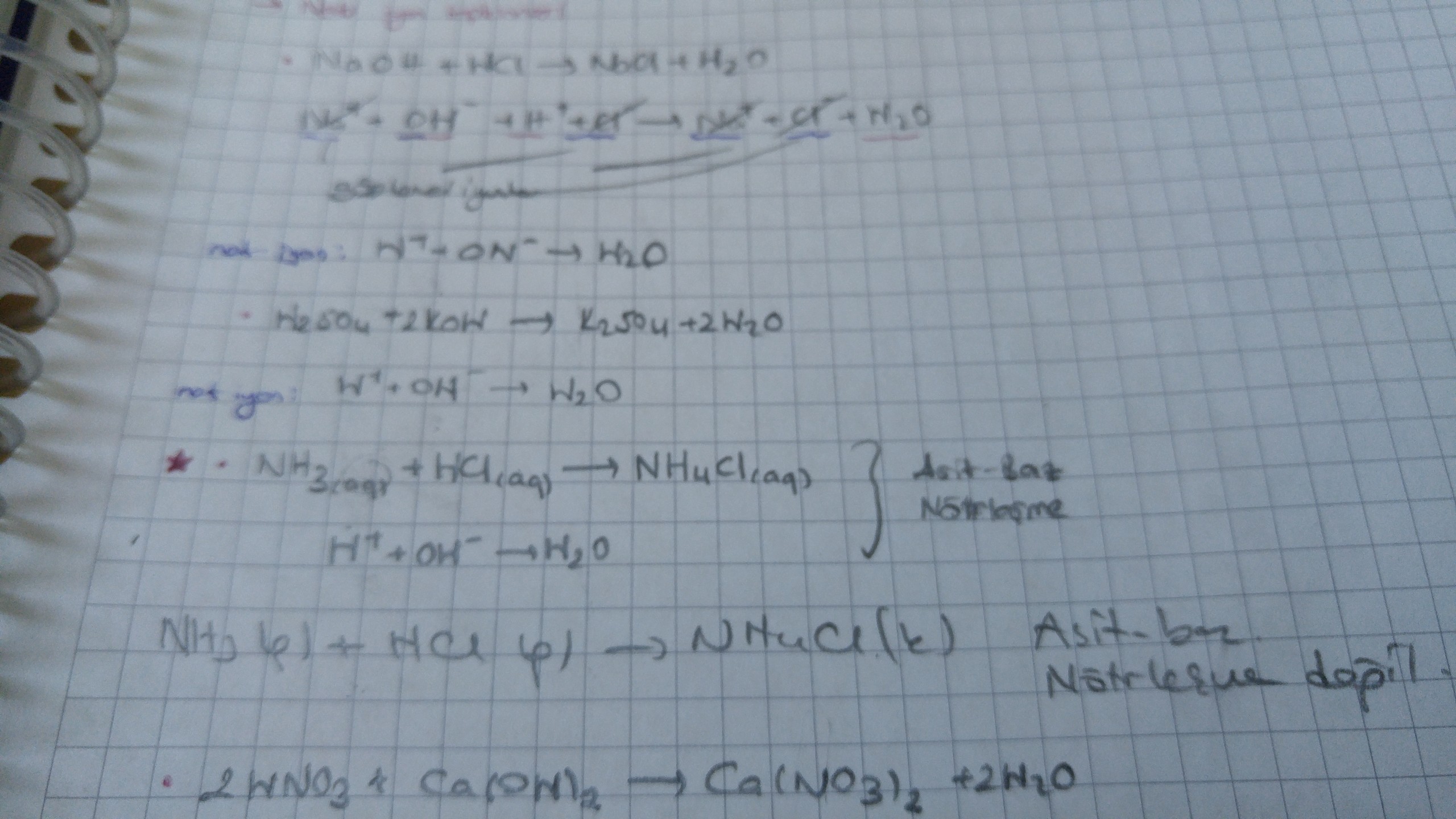Amonyak Formülü - Amonyak Asit Mi, Baz Mı, Formülü Nedir, Nasıl Bulunur Ve Hesaplanır? - Son Dakika Eğitim Haberleri

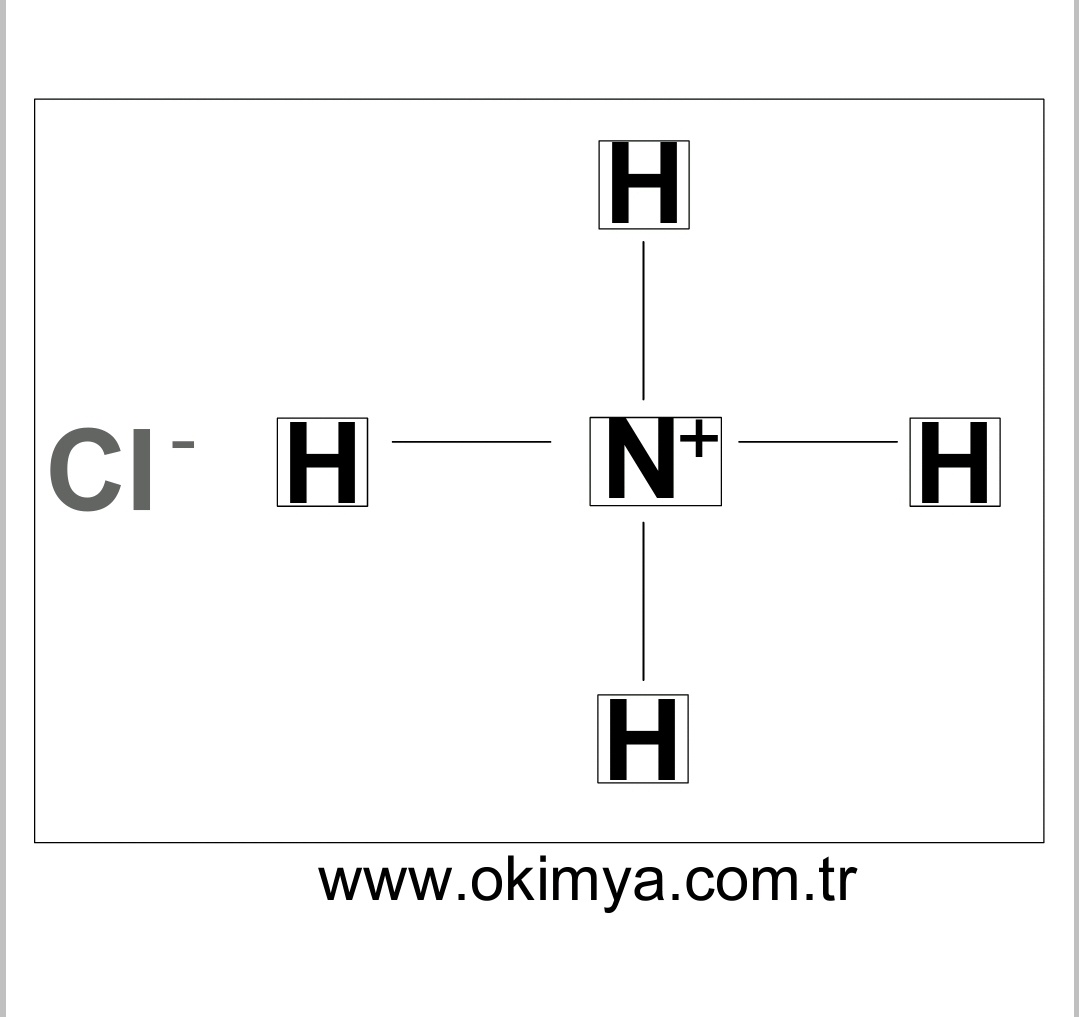
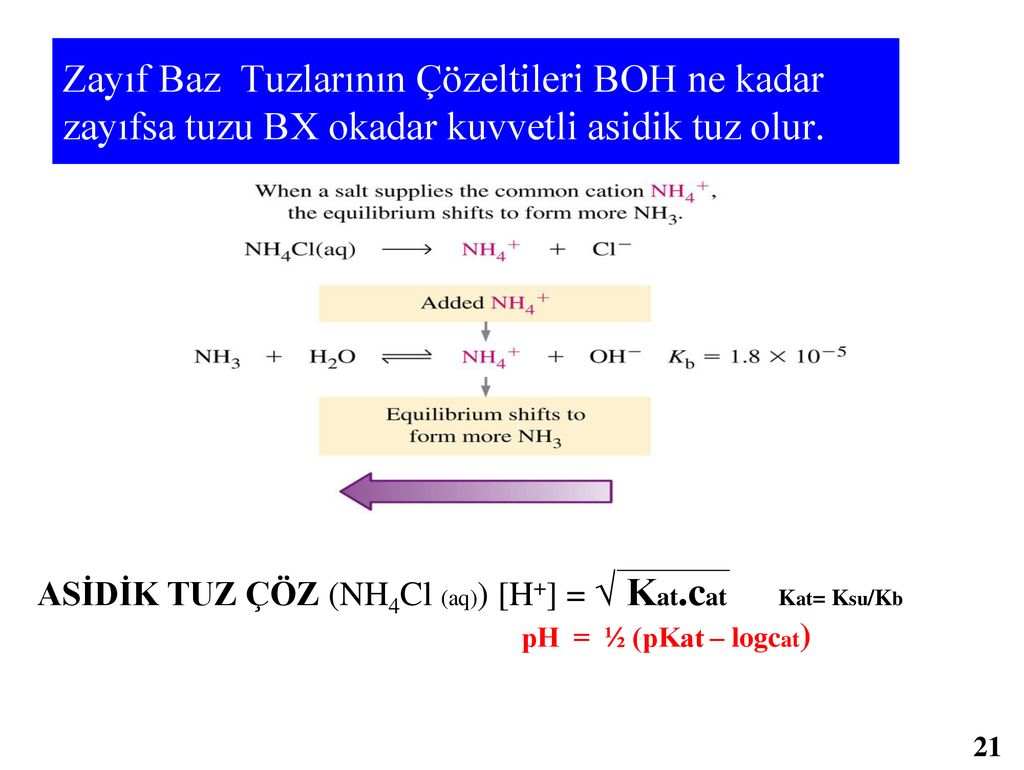
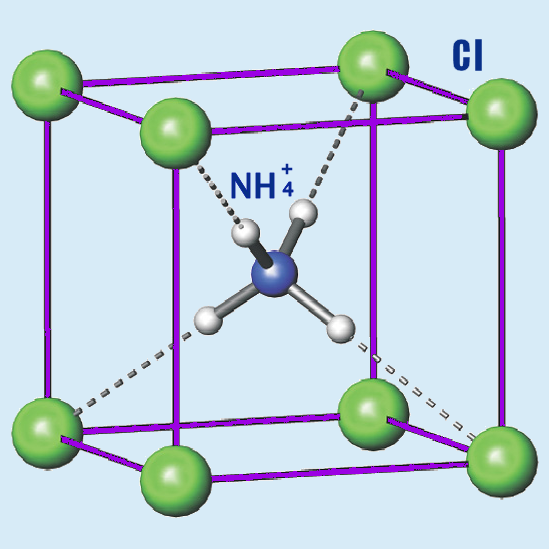
Tuzlar-2 Nişader 9. Amonyum klorür (NH4CI) tuzunun suda çözünme denkle- mi aşağıdaki gibidir. NH4Cl + H₂O - — Buna göre, oluşan çözeltiyle ilgili; → NH3 + H3O+ + Cl¯ \I. Asit özelliği

Aşağıdaki tepkimelerin hangisi nötralleşme tepkimesidir? A) NH3(g) + HCl(g) NH4Cl(k) B) CH4(g) + 2O2(g) - Eodev.com

Asit baz tepkimelerinfe reaktiflerden en az biri suda ise tepkime aynı zamanda nötrleşme tepkimesidir 👍✨ #kimyadersnotları #kim... | Instagram

NH3(suda) + HCl(suda) = NH4Cl(suda) tepkimesi ile ilgili, I. Asit ve baz maddeler arasında gerçekleşir. II. Elektron alışverişi ile oluşur. III. NH4Cl bir tuzdur. IV. Son durumda çözelti elektriği iletmez. yargılarından hangileri

21. Aşağıda oda koşullarında bir asit-baz tepkimesi verilmiştir. NH3(suda) + HCl(suda) - NH4Cl(suda) Kayıf baz Kuvvetli asit Tuz Buna göre, tepkimede oluşan tuz ile ilgili I. Anyonu hidrolize uğrar. Tuz çözeltisinin pH

NH3(suda) + HCl(suda) = NH4Cl(suda) tepkimesi ile ilgili, I. Asit ve baz maddeler arasında gerçekleşir. II. Elektron alışverişi ile oluşur. III. NH4Cl bir tuzdur. IV. Son durumda çözelti elektriği iletmez. yargılarından hangileri
Sodyum Karbonat Nedir ? | Sodyum Karbonat Formülü ? | Sodyum Karbonat Ne İşe Yarar ? | Sodyum Karbonat İçilir Mi ?

TYT Kimya Konu Anlatım Modülleri Modül 4 Karışımlar Asitler, Bazlar ve Tuzlar Kimya Her yerde - Yalnız iii-Iii buna göre-ModÜl tyt Örnek | PubHTML5